 이미지 확대보기
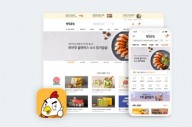
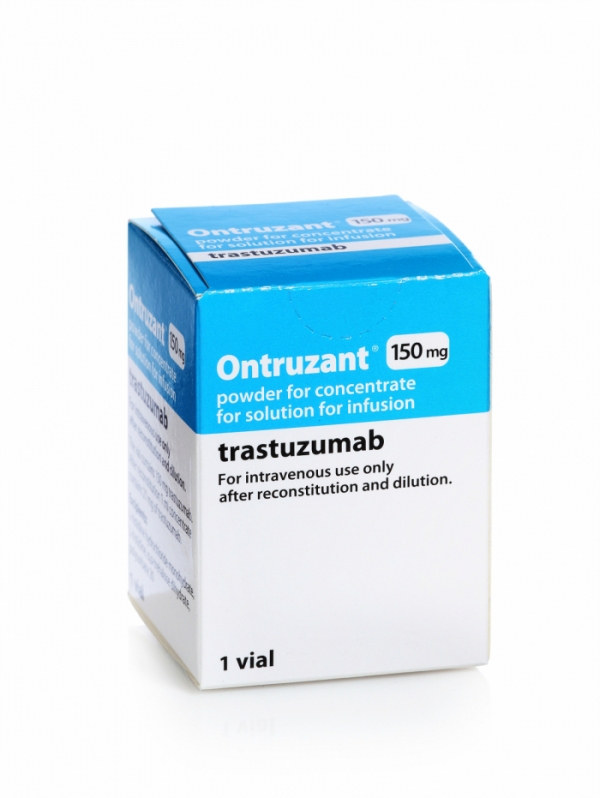
이미지 확대보기FDA는 지난 18일(현지시간) 삼성바이오에피스의 '허셉티' 바이오시밀러 온트루잔트의 판매 허가를 승인했다고 21일 밝혔다.
삼성바이오에피스는 이번 승인을 통해 기존 유럽 시장에 이어 미국 시장에 진출할 수 있게 됐다.
허셉틴은 초기 유방암, 전이성 유방암 및 전이성 위암 치료제다. 지난 2017년 기준 약 8조 원의 매출을 기록한 글로벌 판매 5위 의약품이다. 미국 시장은 3조 원 규모에 달한다.
삼성바이오에피스는 유럽에서 이미 온트루잔트의 판매허가를 얻어 MSD를 통해 판매 중이다. 지난해 미국에서 열린 종양학회 및 유방암 심포지엄에서 3상 임상의 추적결과를 발표, 온트루잔트와 허셉틴 간의 생존율 측면에서 유사성을 입증했다.
한편, 삼성바이오에피스는 ‘휴미라’ 바이오시밀러 ‘임랄디’(성분명 아달리무맙)의 바이오의약품 품목허가신청서를 FDA에 제출했으며, 지난해 9월부터 서류 심사 중이다.
김혜림 기자 hr0731@g-enews.com





























![[초점] 머스크, ‘사이버트럭 일시 생산 중단’ 이유 밝혀](https://nimage.g-enews.com/phpwas/restmb_setimgmake.php?w=80&h=60&m=1&simg=20240419114320069429a1f3094311109215171.jpg)