 이미지 확대보기
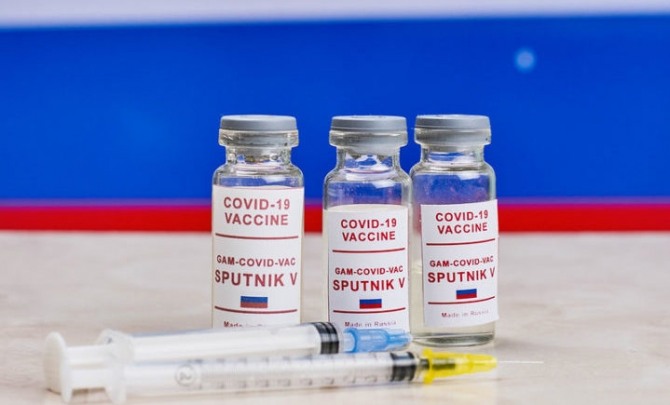
이미지 확대보기네이처는 그러면서 백신 개발 역사가 70년이 넘는 러시아의 스푸트니크V 백신이 여러 논란 속에서 이번엔 거의 드러나지 않은 부작용과 관련, 품질 감시에 의구심이 제기되고 있다고 전했다.
효능과 안전성은 점차 확인되는데, 품질 관리 등에 대한 의혹은 여전하다는 것이다.
스푸트니크V 백신은 러시아 가말레야 연구소에서 개발된 신종 코로나바이러스 감염증(코로나19) 백신이다.
네이처에 따르면 스푸트니크V 백신은 지난해 임상시험 결과가 완전히 공개되지 전에 러시아 정부가 사용을 허가한 이후 일부의 기대 속에 의구심을 야기하며 논란의 대상이 됐다.
스푸트니크V 백신은 67개국에서 승인받았지만, 세계보건기구(WHO)와 유럽의약품청(EMA) 등에서 긴급사용을 승인받지 못했다.
1회 투여로 면역 기능이 형성되는 것으로 알려진 스푸트니크 라이트 백신도 WHO와 EMA 등에서 승인을 받지 못한 상태다.
코백스 퍼실리티 등을 통한 백신을 국제사회에 공급하기 위해서는 WHO 승인이 필수적이다.
러시아는 앞서 지난해 8월 11일 스푸트니크V 백신의 사용을 승인했다.
말레야 연구소가 임상 1차와 2차 시험 데이터를 공개하기 1개월 전이었다.
전문가들은 일련의 비판해 왔다.
호주 버넷연구소의 전염병학자 마이클 툴은 “임상시험 결과가 공개되기도 전에 이뤄진 백신에 대한 긴급사용 승인은 신뢰를 쌓기 힘들다”고 직격했다.
과학자들은 지난 2월 공개된 스푸트니크v의 감영 예방 효과 91.6%에 대해서도 의구심을 제기했다.
최초 데이터가 공개되지 않고 있어 제대로 내용을 파악하기 힘들기 때문이다.
부작용이 전혀 없다는 것도 의구심을 낳고 있다고 네이처는 전했다.
아데노바이러스 백신을 활용하는 아스트라제네카와 존슨앤드존슨(얀센) 등은 혈전 관련 부작용 사례가 나오고 있지만, 스푸트니크V 백신은 이런 사례가 전혀 보고되지 않고 있다.
이런 상황에서 WHO는 가말리야 연구소에 추가 데이터를 요청했다. 임상시험 관련 내용도 살피면서, 현재까지 9개 현장을 점검했다.
EMA의 승인절차도 진행되고 있지만, 확실한 답은 나오지 않고 있다.
러시아 측은 스푸트니크V 백신에 대한 승인이 지연되고 있다며, 여기에는 정치적인 의도가 개입돼 있다고 비판하고 있다.
정작 러시아에서는 지난 6월 28일 기준으로 전체 인구 1억4000만 명 가운데 15%만이 백신을 접종했다고 네이처는 밝혔다.
유명현 글로벌이코노믹 기자 mhyoo@g-enews.com


























![[초점] 스텔란티스, 트럼프 고율 관세에 美 자동차 부품공장 5곳...](https://nimage.g-enews.com/phpwas/restmb_setimgmake.php?w=80&h=60&m=1&simg=20250404155804082389a1f3094311109215171.jpg)














